Un glaçon qui résonne dans un verre, la buée qui dessine des formes sur la vitre, la casserole qui "chante" quand l'eau se met à bouillir... On les voit tous les jours, mais on ne les explique pas toujours. Et pourtant, ces petites scènes de vie racontent la grande histoire des trois états de la matière : solide, liquide et gaz.
Dans cet article, on va démystifier ces notions avec des mots simples, des images parlantes et des expériences faciles à faire à la maison. Tu pourras expliquer à ton enfant comment l'eau passe de la glace à la vapeur d'eau, pourquoi la buée apparaît après la douche, ou encore pourquoi la cocotte-minute cuit plus vite. Prêt·e à jouer les scientifiques du quotidien ?
Les états de la matière en 2 minutes
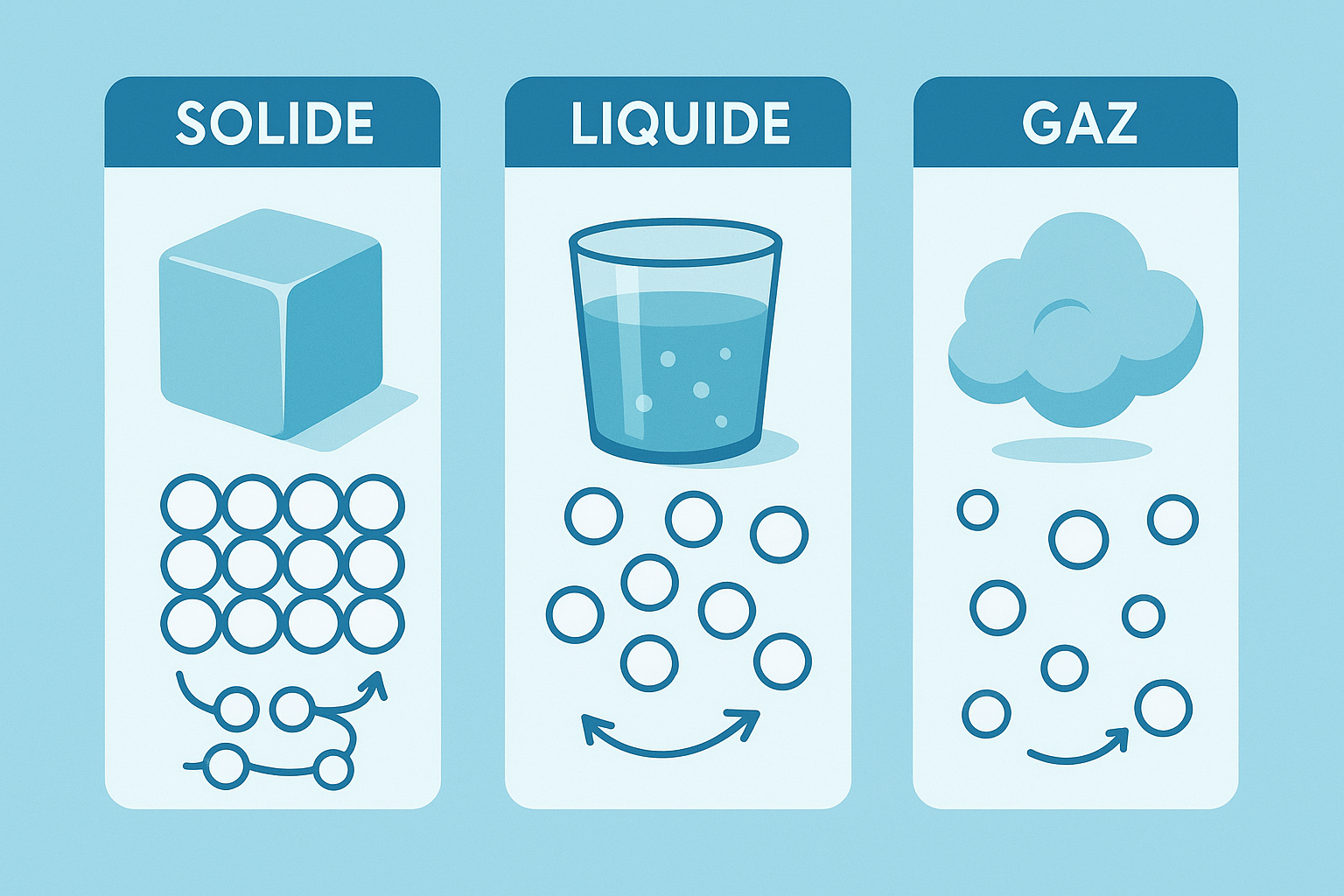
Définition simple : solide, liquide, gaz
- Solide : les particules (minuscules "billes") sont très proches et presque immobiles ; l'objet garde sa forme (un glaçon, un caillou, un cube de sucre).
- Liquide : les particules sont proches mais libres de glisser les unes sur les autres ; le liquide prend la forme du récipient (un verre d'eau, du lait, de l'huile).
- Gaz : les particules sont très espacées et rapides ; le gaz occupe tout l'espace disponible (la vapeur d'eau, l'air que l'on respire).
En une phrase : plus on chauffe, plus ça bouge ; plus ça bouge, plus la matière a tendance à "se libérer" de sa forme.
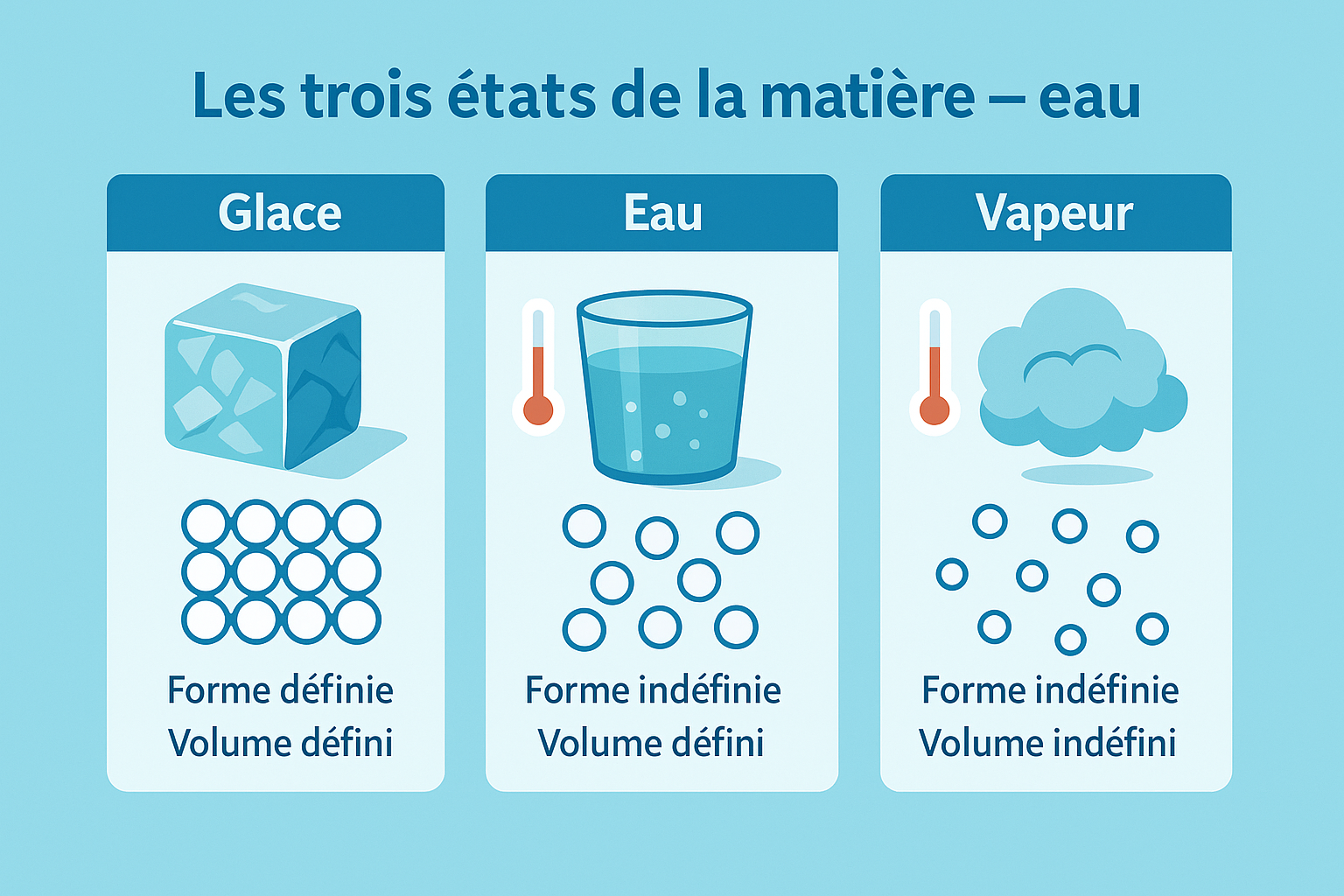
Exemples concrets avec l'eau (glace, eau, vapeur)
L'eau est la star pédagogique :
- Glace (solide) au congélateur,
- Eau liquide dans ton verre,
- Vapeur d'eau (gaz) au-dessus d'une casserole qui bout.
Tu as donc sous la main un laboratoire miniature pour tout montrer sans jargon.
Pourquoi l'eau est un super "prof" de sciences pour enfants
- Elle change d'état dans une plage de températures faciles à obtenir (0 °C et 100 °C à la pression du niveau de la mer).
- Elle est non toxique, disponible et sécurisante (avec les précautions de base).
- Elle illustre le cycle naturel (nuages -> pluie -> rivières -> évaporation). Voir aussi formation de la pluie et de la neige.
Ce qui se passe "à l'intérieur" : la danse des particules
Agitation thermique : plus c'est chaud, plus ça bouge
Imagine des enfants sur une piste de danse. Musique douce ? Tout le monde bouge peu, on reste groupés (état solide). La musique accélère ? On se déplace, on se frôle, on change de place (état liquide). La musique devient folle ? Chacun part dans tous les sens, l'espace se remplit (état gaz). C'est exactement l'effet de la température sur l'agitation des particules.
Liaisons et forces entre molécules : quand ça colle... ou pas
Dans la glace, les molécules d'eau (H?O) s'ordonnent comme dans un cristal ; elles se "tiennent la main" si fort que la forme est rigide. Dans l'eau liquide, elles gardent des contacts mais glissent : c'est fluide. Dans la vapeur, elles s'éloignent largement, les forces d'attraction ne suffisent plus pour les maintenir ensemble. Retenir l'idée : chauffe = énergie ajoutée -> les particules se libèrent.
Énergie absorbée vs. libérée (endothermique / exothermique) expliqué sans jargon
- Endothermique : le système absorbe de l'énergie (par ex. la fusion : faire fondre la glace demande de l'énergie).
- Exothermique : le système libère de l'énergie (par ex. la solidification : l'eau qui gèle libère de la chaleur).
Cette clé explique pourquoi la main sent du froid quand un liquide s'évapore à sa surface (l'évaporation pompe de l'énergie et refroidit localement). Pour aller plus loin côté énergie thermique, découvre énergie solaire et chaleur.
Les changements d'état : le grand carrousel de l'eau
Fusion et solidification (0 °C)
- Fusion : glace -> eau liquide. Elle commence à 0 °C (au niveau de la mer), mais il faut fournir de la chaleur pour faire fondre tout le glaçon.
- Solidification : eau liquide -> glace. Le processus inverse libère de l'énergie.
Astuce parent
Pour faire fondre un glaçon plus vite, augmente les échanges de chaleur : eau tiède, contact avec une surface métallique, ou sel (qui perturbe l'organisation des molécules). Compare aussi densité de l'eau et température.
Vaporisation (ébullition), évaporation et condensation
- Ébullition : eau liquide -> vapeur dans tout le volume à une température d'ébullition (100 °C au niveau de la mer). Les bulles, c'est du gaz qui se forme à l'intérieur.
- Évaporation : passage en gaz uniquement à la surface, même en dessous de 100 °C. Un t-shirt qui sèche au soleil, c'est de l'évaporation.
- Condensation : vapeur -> liquide (la buée sur le miroir, la rosée du matin). Voir l'article expériences scientifiques faciles pour enfants.
Sublimation et condensation solide : la "magie" du givre
- Sublimation : solide -> gaz sans passer par le liquide (ex. : la glace qui "disparaît" lentement dans un congélateur très sec).
- Condensation solide (ou dépôt) : gaz -> solide (ex. : givre qui se forme directement à partir de la vapeur d'eau sur une surface froide). Pour des idées d'atelier hiver : expériences sur la neige.
Schéma récapitulatif simple
(Sublimation) (Condensation solide)
Glace (solide) <----------------> Vapeur (gaz)
| (Fusion) (Solidification) |
v ^
Eau (liquide) --(Vaporisation/Ébullition)-->
^ (Condensation) |
|---------------(Évaporation)------------|
Température, pression... et altitude : pourquoi l'eau ne bout pas toujours à 100 °C
Point d'ébullition qui change avec la pression (montagne vs. mer)
L'ébullition survient quand la pression de vapeur de l'eau égale la pression extérieure. En altitude, la pression atmosphérique est plus faible, donc l'eau bout plus tôt... mais à une température plus basse (par ex. ~95 °C vers 1 500-2 000 m). Résultat : les pâtes cuisent plus lentement à la montagne.
Diagramme de phases de l'eau (point triple, point critique) vulgarisé
Imagine une carte avec 2 axes : température (horizontale) et pression (verticale). Selon l'endroit où tu te trouves, l'eau est solide, liquide ou gaz.
- Point triple : l'eau peut coexister sous les trois états (solide, liquide, gaz).
- Point critique : au-delà, la distinction liquide/gaz s'efface ; on parle de fluide supercritique.
Applications du quotidien (cocotte-minute, météo)
- Cocotte-minute : elle augmente la pression, donc la température d'ébullition ; la cuisson est plus rapide. Découvre aussi énergie solaire et chaleur.
- Météo : la formation des nuages dépend de la température et de la pression ; la vapeur se condense en micro-gouttelettes quand l'air se refroidit. À relier avec pourquoi le ciel est bleu et couleurs de l'arc-en-ciel.
Les états de la matière dans la vraie vie
Cuisine : glaçons, sauces, vapeur de cuisson
- Glaçons pour refroidir (solidification).
- Épaississement d'une sauce : l'eau s'évapore, la sauce réduit.
- Vapeur pour cuire en douceur : condensation sur l'aliment = chaleur libérée, cuisson efficace.
Météo : nuages, pluie, neige, buée
- Nuages : gouttelettes liquides en suspension (non, ce n'est pas de la vapeur "visible").
- Pluie : gouttes assez lourdes pour tomber.
- Neige : cristaux solides.
- Buée sur les vitres : condensation de la vapeur sur une surface froide. Voir formation de la pluie et de la neige.
Maison & jeux d'observation
- Bouteille sortie du frigo : gouttelettes qui apparaissent = condensation.
- Miroir de salle de bain : la surface froide capte la vapeur.
- Sèche-linge : accélère l'évaporation (air chaud et brassage).
5 expériences faciles et sûres à faire avec un enfant
Rappel sécurité : manipule l'eau chaude avec prudence, supervise en permanence, privilégie la plaque plutôt que le gaz, et attends le refroidissement avant de manipuler.
1) "Nuage en bocal" (condensation) -- nuage en bocal tuto
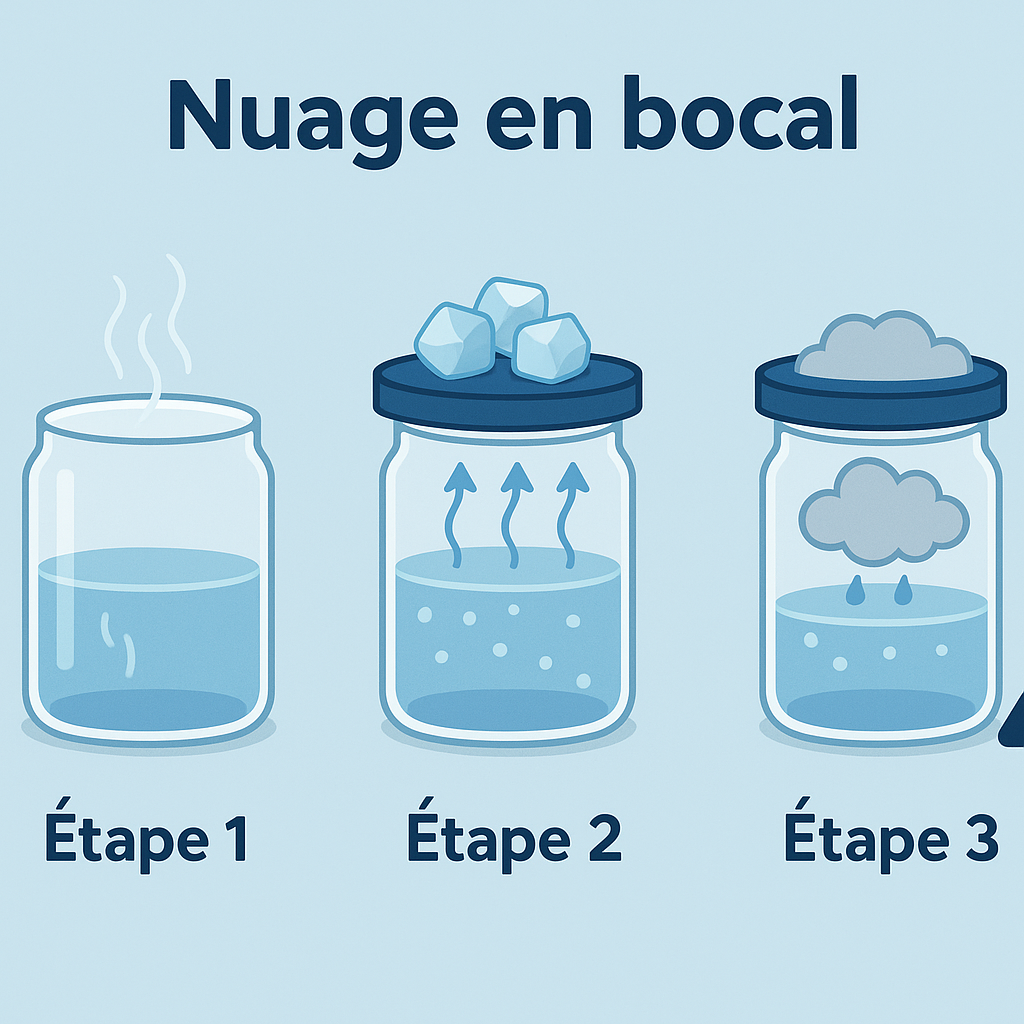
Matériel
Un pot en verre avec couvercle, eau très chaude, glaçons.
Étapes
- Verse un fond d'eau chaude dans le pot, referme.
- Pose quelques glaçons sur le couvercle (mets un petit bol pour les maintenir).
- Observe : la vapeur chaude monte, touche le couvercle froid, condense -> un "nuage" apparaît.
Ce qu'on apprend
Vapeur -> liquide quand l'air est refroidi (condensation), comme dans un nuage réel. À rapprocher de expériences scientifiques faciles pour enfants.
2) "Glace instantanée" (eau surfondue, version simple et sans risque)
Idée
Montrer qu'un liquide peut geler d'un coup si on déclenche la cristallisation.
Méthode accessible
- Mets au congélateur 2 bouteilles d'eau plate à l'horizontale pendant ~2 h 15 à 2 h 30 (selon congélateur).
- Sors délicatement : l'eau est très froide mais encore liquide (surfusion).
- Verse sur un petit glaçon : la glace se forme instantanément en cascade.
Message
Les impuretés ou une graine (le glaçon) déclenchent la cristallisation.
3) "La pluie dans un verre" (cycle miniature)
Matériel
Un grand verre transparent, de l'eau très chaude, une assiette froide, quelques glaçons.
Étapes
- Remplis le verre d'eau très chaude (3/4).
- Pose l'assiette froide au-dessus (avec 3-4 glaçons dessus).
- Observe les gouttelettes se former et tomber comme une pluie miniature.
Concepts
Évaporation (eau chaude), condensation sous l'assiette froide, précipitation (les gouttes tombent). Complément : formation de la pluie et de la neige.
4) "Vapeur qui devient gouttes" (piège à vapeur)
Matériel
Casserole, couvercle en verre incliné, bol sous le bord, eau chaude.
Étapes
- Porte l'eau à frémissement (pas besoin d'ébullition).
- Place le couvercle en biais pour que la vapeur condense sur la face interne et s'écoule vers un point.
- Place un bol pour collecter l'eau qui goutte.
Intérêt
Visualiser vapeur -> liquide et discuter de la distillation (version maison, simplifiée). Idées liées : expériences scientifiques faciles pour enfants.
5) "Sublimation du givre" (observation guidée)
Matériel
Une plaque métallique (ou une cuillère), un congélateur, une lampe de poche.
Étapes
- Laisse la plaque se couvrir de givre dans le congélateur.
- Sors-la dans une pièce très sèche (ou près d'un courant d'air) et observe le givre disparaître sans fondre en flaques.
Conclusion
Une partie du givre peut sublimer (solide -> gaz) si l'air est sec et un peu plus chaud.
Conseil "classe"
Photographier chaque étape et demander à l'enfant d'étiqueter le changement d'état (fusion, condensation, etc.). Excellent pour le vocabulaire. Pour varier, essaie cette expérience de capillarité.
Erreurs fréquentes et idées reçues
"L'eau bout toujours à 100 °C" (faux)
Vrai au niveau de la mer ; en altitude, moins. Dans une cocotte-minute, plus.
"La vapeur est visible"
La vapeur pure est invisible ; ce que tu vois au-dessus de la casserole, ce sont des micro-gouttelettes liquides formées par condensation. D'où l'apparence "blanchâtre".
"Ébullition = évaporation"
Non : l'ébullition se produit dans tout le volume à la température d'ébullition, l'évaporation est un phénomène de surface et peut avoir lieu bien en dessous.
Fiches pratiques pour parents & enseignants
Pédagogie par l'expérience : déroulé de séance MS-GS / CP-CE2 / CM1-CM2
MS-GS (maternelle)
- Objectif : nommer les 3 états, reconnaître "glace/eau/vapeur".
- Activités : toucher de la glace, observer de la buée sur un miroir, regarder une casserole qui fume (à distance).
- Langage : "dur / liquide / fumée d'eau", "ça fond / ça disparaît en air".
- Trace : coller des photos dans un ordre logique (glace -> eau -> vapeur).
CP-CE2 (cycle 2)
- Objectif : décrire les changements d'état (fusion, évaporation, condensation).
- Activités : "Nuage en bocal", "Pluie dans un verre", glaçon qui fond sur différentes surfaces.
- Langage : fusion, condensation, évaporation, température.
- Trace : flèches sur un schéma avec les mots exacts.
CM1-CM2 (cycle 3)
- Objectif : relier température/pression aux changements d'état, distinguer évaporation/ébullition.
- Activités : mesurer la température à différents moments (thermomètre), comparer altitude (lecture d'un tableau), cocotte-minute : comment ça marche (schéma).
- Langage : point d'ébullition, pression, diagramme de phases (intro), endothermique/exothermique. Ressource utile : expériences scientifiques faciles pour enfants.
Vocabulaire visuel (affiche / mini-quiz)
- Solide - Liquide - Gaz
- Fusion, Solidification, Vaporisation/Ébullition, Évaporation, Condensation, Sublimation, Condensation solide
Quiz rapide
- La buée sur la vitre, c'est... (condensation)
- Un t-shirt qui sèche, c'est... (évaporation)
- Un glaçon qui fond, c'est... (fusion)
- Neige qui se forme dans l'air froid : condensation solide
- Eau qui bout en montagne : ébullition à température plus basse
Évaluation rapide : 10 questions pour vérifier la compréhension
- Cite les trois états de la matière.
- Donne un exemple de chaque état avec l'eau.
- Qu'appelle-t-on fusion ? Et solidification ?
- Quelle est la différence entre évaporation et ébullition ?
- Pourquoi une cocotte-minute cuit plus vite ?
- Que se passe-t-il si on augmente l'altitude ? (température d'ébullition ?)
- La vapeur est-elle visible ? Explique.
- Donne une situation de condensation dans la maison.
- Qu'est-ce que la sublimation ?
- Relie endothermique/exothermique à un exemple (fusion, solidification).
Conclusion
Tu l'as vu, les états de la matière ne sont pas qu'une leçon de science : c'est un spectacle permanent autour de nous. Avec un peu d'observation et quelques expériences, un enfant comprend vite comment l'eau passe de la glace à la vapeur d'eau, pourquoi la buée apparaît, et comment la pression change les règles du jeu.
Le mieux ? Choisir une des expériences ci-dessus, la faire maintenant, puis demander à ton enfant de raconter ce qu'il a vu : "Ça a fondu ? Ça s'est évaporé ? Ça a condensé ?" C'est comme ça qu'on ancre les notions, sans s'en rendre compte. À toi de jouer ! Pour prolonger à la maison, découvre aussi jeux d'eau faciles et jeux d'eau pour enfants.
FAQ (optimisée SEO)
Pourquoi la glace flotte-t-elle sur l'eau ?
Parce que la glace a une densité plus faible que l'eau liquide : sa structure cristalline occupe plus d'espace pour la même masse, donc elle flotte.
À quelle température l'eau bout-elle en montagne ?
Plus l'altitude est élevée, plus la pression atmosphérique baisse et plus la température d'ébullition diminue (autour de 95 °C vers 1 500-2 000 m). La cuisson est donc plus lente.
Quelle est la différence entre évaporation et ébullition ?
L'évaporation a lieu à la surface, à toute température ; l'ébullition se produit dans tout le liquide à la température d'ébullition.
La vapeur d'eau est-elle visible ?
La vapeur pure est invisible. Le "nuage blanc" au-dessus d'une casserole, ce sont des micro-gouttelettes liquides formées par condensation.
Pourquoi la buée apparaît-elle sur un miroir ?
La vapeur d'eau de l'air se condense sur le miroir froid : elle devient de fines gouttelettes qui diffusent la lumière.
Comment expliquer les états de la matière à un enfant ?
Utilise l'eau (glace/eau/vapeur) et des gestes : toucher, observer la fonte, collecter la condensation. Nomme chaque changement d'état au moment où il se produit.
Cocotte-minute : comment ça marche ?
Elle augmente la pression interne, ce qui élève la température d'ébullition de l'eau. La nourriture cuit plus vite à plus haute température.
Sublimation : un exemple simple ?
Le givre qui "disparaît" au contact d'un air sec et un peu plus chaud : le solide passe directement en gaz.












